AMD - en sygdom i øjet og immunsystemet
Kan vi behandle tidlig AMD med immun-regulerende medicin i øjet?
Hvad er AMD?
Aldersrelateret Makula Degeneration (AMD), også kaldet alderspletter på nethinden, er den vigtigste årsag til svagsyn og social blindhed i Danmark og resten af Vesten. Den rammer i helt overvejende grad folk over 60 år, og oftest er patienter med sene stadier af sygdommen over 75 år. Sygdommen starter med alderspletter, kaldet druser, der er en ophobning af små mængder affaldsstoffer bestående af protein (æggehvidestof) og fedt. Patienten kan gå med disse druser i årevis, og nogle udvikler
aldrig de senere stadier af sygdommen, mens druser hos andre i sidste ende resulterer i læseblindhed
(synsstyrke < 6/60 ~ < 0,1).
Hvad skyldes AMD?
Vi kender stadig ikke årsagen til, at nogle mennesker udvikler AMD. Gennem de seneste 10 år er det dog blevet klart, at immunsystemet - kroppens indbyggede værn mod infektioner - er involveret i sygdommen. Genetiske studier har vist, at mutationer i gener, der koder for den del af immunforsvaret, der kaldes komplement-systemet, giver øget risiko for at udvikle AMD. Derudover har forskere fundet en lang række immun-relaterede proteiner i druser.
Hvordan udvikles AMD?
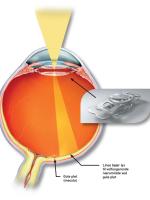
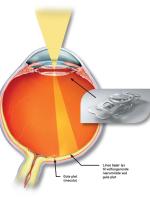
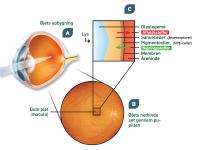
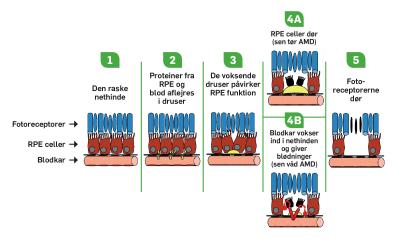
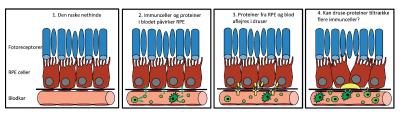
I den bageste del af øjet, nethinden, sidder de sanseceller, der sender besked til hjernen om, hvad øjet ser (Fig.1). Disse sanseceller kaldes fotoreceptorer, fordi de absorberer lyset. Fotoreceptorerne er højt specialiserede og har brug for støtte fra andre celler til at ordne dagligdags funktioner som at optage næring og få fjernet affaldsstoffer. Disse støtteceller kaldes retinale pigment epitel - RPE-celler (Fig. 1). Når der ophobes druser i nethinden, påvirker det RPE-cellerne, som derved får svært ved at skabe optimale forhold for fotoreceptorerne. Resultatet er, at både RPE-celler og fotoreceptorer langsomt dør (såkaldt sen tør AMD). I nogle tilfælde invaderer små blodkar nethinden og giver en pludselig ødelæggelse af nethinden (sen våd AMD, Fig.2).
Der findes ingen helbredende behandling for AMD
Tør AMD giver langsomt et forværret syn, mens våd AMD ofte giver pludselig synsnedsættelse. I dag forebygges sen AMD ved at give et høj-dosis tilskud af en række vitaminer og mineraler. Dette kan forebygge, at druserne vokser, og muligvis gøre RPE-cellerne mere modstandsdygtige. Ved fremskreden AMD, hvor RPE-celler og fotoreceptorer er døde, findes der ingen behandling. Hverken RPE-celler eller fotoreceptorer kan gendanne sig, og derfor er disse skader blivende. Ved sen våd AMD kan man forsinke sygdommens fremskriden ved at give indsprøjtninger ind i øjet, som hæmmer dannelsen af blodkar. Dette fjerner dog ikke den underliggende sygdom, som stadig udvikler sig langsomt.
Forebyggelse frem for behandling
Når først RPE-celler og fotoreceptorer er døde, er det hidtil umuligt at erstatte dem. Der har de seneste 30 år været mange forsøg på transplantation af celler til nethinden, men hidtil uden succes. En anden fremgangsmåde er at sætte ind før nethindens celler dør, altså ved forebyggelse. Da druserne ofte fremkommer 10-20 år før patienten udvikler tør eller våd AMD, vil det være nærliggende at starte en forebyggende behandling tidligt. Men hvorfor får vi druser?
Druser stammer fra både blodet og nethinden
Det spørgsmål har forskere forsøgt at komme nærmere et svar på ved at udtage druser fra afdøde med AMD og undersøge indholdet af proteiner og fedtstoffer. Ud fra disse studier ved vi, at druser indeholder nogle stoffer, der stammer fra blodet og andre, der stammer fra nethinden. Dette fortæller os, at sygdommen ikke kun sidder i øjet, men at den måske starter et helt andet sted.
Det aldrende immunsystem
Når vi bliver ældre, sker der en masse forandringer i kroppen. Nogle er nemme at opdage - vi får rynker og gråt hår - mens andre er mere skjulte. Vores blod indeholder hovedsagelig røde blodceller, der transporterer ilt, og hvide blodceller, som udgør vores immunsystem. Hvis vi bliver smittet med en bakterie, bliver immunsystemet aktiveret og begynder straks at bekæmpe bakterien. En af de skjulte aldersforandringer er de store omvæltninger, der sker i immunsystemet, når man bliver ældre. De betyder, at vi ikke længere er så gode til at bekæmpe nye infektioner, som for eksempel influenzavirus.
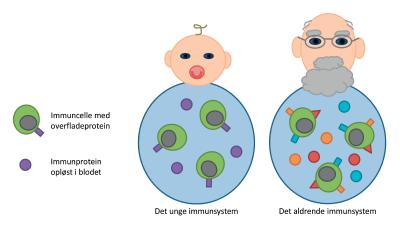
For at kompensere for dette, laver immunsystemet nogle ændringer i sammensætningen af proteiner i blodet og på overfladen af immuncellerne (Fig. 3). Disse ændringer betyder, at der ikke kræves så meget, før immuncellerne bliver aktiveret og går til angreb på for eksempel bakterier eller vira. Desværre kan ændringerne også bevirke, at immuncellerne bliver sværere at kontrollere og cirkulerer rundt i en mere aktiveret tilstand, hvilket kan være til skade for kroppen.
Immunsystemet er forandret i patienter med AMD
Øjenafdelingen på Roskilde Sygehus indsamler blodprøver fra patienter med AMD for at undersøge deres immunsystem. I samarbejde med forskergruppen i Roskilde undersøger vi tilstedeværelsen af en lang række overfladeproteiner på immuncellerne og opløselige proteiner i blodet. Selv om indsamlingen af blodprøver endnu er i gang, har vi allerede fundet flere ændringer i AMD patienters immunceller og blod, sammenlignet med raske personer i samme alder.
Et for aktivt immunsystem kan være skadeligt
Vi ved endnu ikke med sikkerhed, hvad disse immunologiske ændringer præcist betyder, og hvordan de forårsager AMD. Men samlet set tyder det på, at immunceller i AMD patienter er lettere at aktivere - og dermed - at de lettere kan gå til angreb på bakterier og måske også kroppens egne celler. Man kan sammenligne det med en pistol: hos raske ældre er pistolen ikke ladt, og det tager derfor et øjeblik længere at skyde, hvis man ser noget mistænkeligt. Man kan så at sige nå at tænke sig om inden affyring. Hos AMD patienter er pistolen ladt og klar til skud, og man risikerer derfor at ramme uskyldige.
Mus som model for mennesker
Vi forsøger nu at komme nærmere et svar på, om et for aktivt immunsystem direkte kan påvirke øjencellerne. Vi har undersøgt øjnene fra mus inficeret med et virus, som giver kraftig aktivering af immunsystemet.
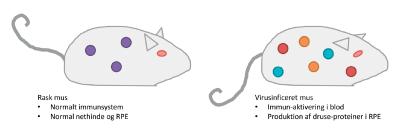
Nethinden i virus-inficerede mus viste klare tegn på at være påvirket af det aktiverede immunsystem (Fig. 4). RPE-cellerne fra musene viste også en øget aktivering af de gener, som koder for druse-proteiner, proteiner, der også kan aktivere immunsystemet yderligere. Dette resultat understøtter hypotesen om, at et for aktivt immunsystem kan påvirke og muligvis forårsage skade i nethinden.
Celler som model for mennesker
For at komme endnu dybere ned i mekanismen bag immunsystemets effekt på RPE celler og udviklingen af AMD, har vi stillet endnu en model op.
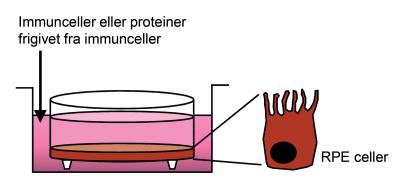
Vi bruger en RPE-cellelinje, som vi dyrker i små skåle i et varmeskab (Fig. 5). Når vi behandler cellerne med proteiner, der bliver frigivet af aktiverede immunceller, kan vi måle RPE-celledød. Dette indikerer, at immun-aktivering kan være med til at stresse RPE-cellerne.
Men udover direkte at forårsage RPE-celledød, får disse immun-aktiverende proteiner også RPE-cellerne til at producere en lang række proteiner (Fig. 6). Ligesom hos musene, er mange af disse proteiner fundet aflejret i druser hos afdøde og kan potentielt tiltrække og aktivere immunceller.
Kan RPE celler tiltrække immunceller?
Vi er nu i gang med at undersøge præcis, hvordan immunsystemet påvirkes, når det møder blandingen af disse stoffer produceret af RPE-cellerne. Hvordan påvirkes aktiveringen af lokale immun-proteiner? Bliver flere immunceller tiltrukket til området? I hvilken grad bliver de aktiveret? Øget immun-aktivering ved nethinden kunne resultere i en ond cirkel, hvor et lidt for aktivt immunsystem påvirker RPE-cellerne, som aktiverer immunsystemet yderligere, som derpå påvirker RPE-cellerne yderligere, og så videre.
Konklusion
Vi ved i dag, at immunsystemet er involveret i udviklingen af AMD, men ikke hvordan. Meget tyder på, at øget aktivering af immunsystemet kan forårsage dannelse af proteiner i RPE-cellerne og i blodet, som kan aflejres i form af druser. Disse druse-proteiner kan være medvirkende til øget aktivering af immunsystemet og dermed starte en ond cirkel.
Perspektiver for fremtidens behandling af AMD
Hvis vi forstår hvordan immunsystemet kan forårsage dannelsen af druser og RPE-celledød, kan vi potentielt blokere processen lokalt i øjet uden at påvirke immunsystemet i resten af kroppen. Dermed bliver patientens forsvar mod infektioner ikke nedsat. En øget forståelse af de cellulære mekanismer vil dermed give os meget bedre muligheder for at udvikle en effektiv behandling, der kan sættes ind i de tidlige stadier af AMD. Ved at starte behandlingen tidligt undgår vi ødelæggelse af fotoreceptorerne med synstab til følge.
Forskningen er udført af forskergrupperne på Øjenafdelingen, Roskilde Sygehus og Eye Research Unit, Institut for International Sundhed, Immunologi og Mikrobiologi (ISIM), Københavns Universitet
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.