De sjældne nethindesygdomme (er slet ikke så sjældne endda)
Hver for sig er der tale om små patientgrupper, men tilsammen er der en betydelig andel danskere, der har en arvelig nethindesygdom. Langt de fleste arvelige nethindesygdomme er fremadskridende og fører i værste fald til, at patienterne mister synet. Indtil nu har det skortet på forebyggelses- og behandlingsmuligheder, men nye teknologier giver håb for fremtiden, siger overlæge Line Kessel, der arbejder med patientgruppen.

Line Kessel er overlæge på øjenafdelingen ved Rigshospitalet – Glostrup, og hun har dedikeret store dele af sin karriere til at forske i og arbejde med arvelige nethindesygdomme.
Foto: Joachim Rode
Arvelige nethindesygdomme er en gruppe af degenerative nethindesygdomme, som er forårsaget af en genetisk defekt (mutation). I dag er der identificeret over 250 gener, hvori genetiske defekter kan føre til arvelig nethindesygdom.
Arvelige nethindesygdomme varierer med hensyn til debut og sygdomsforløb, men er overvejende kendetegnet ved et langsomt tab af fotoreceptorer. Den mest udbredte retinale dystrofi er Retinitis Pigmentosa (RP). Arvelige nethindesygdomme er ofte isoleret til øjet, men hos cirka hver fjerde patient er andre organer også påvirket af sygdom.
I Danmark er der omkring 1.600 øjenpatienter, der har en arvelig nethindesygdom. Arvelige nethindesygdomme er degenerative sygdomme i nethinden; altså sygdomme, der nedbryder nethinden. De skyldes fejl i et eller flere gener. I dag er der identificeret over 250 gener, hvori genfejl kan føre til arvelig nethindesygdom. For tre ud af fire patienter er den arvelige nethindesygdom kun lokaliseret i nethinden, men for den sidste fjerdedel af patienterne gælder det, at de også har sygdom andre steder i kroppen, for eksempel i det indre øre eller i nyrerne. Da de fleste arvelige nethindesygdomme er fremadskridende, vil en række patienter opleve, at synet bliver dårligere med årene. I værste fald mister patienterne synet.
Nogle arvelige nethindesygdomme er hurtigt fremadskridende, mens andre udvikler sig langsomt og først giver symptomer efter mange års sygdom. Børn kan også blive ramt af arvelig nethindesygdom. Arvelig nethindesygdom er årsag til 13 pct. af synshandikap blandt danske børn.
”Arvelig nethindesygdom viser sig som oftest tidligt i livet. Da de fleste arvelige nethindesygdomme er fremadskridende, vil det at have arvelig nethindesygdom ofte sætte store begrænsninger for det liv, patienterne kommer til at leve,” siger Line Kessel, der er overlæge på øjenafdelingen ved Rigshospitalet – Glostrup og arbejder med arvelig nethindesygdom.
De eneste stationære arvelige nethindesygdomme, der findes, er den gruppe af sygdomme, der går under betegnelsen akromatopsi. Ved akromatopsi er patienterne født med nedsat syn, da deres tapceller er dysfunktionelle fra fødslen. Der er omkring 100 patienter med akromatopsi i Danmark.
Stav- og tapsygdomme
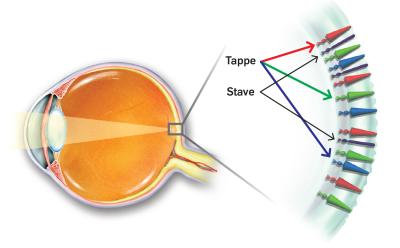
De arvelige nethindesygdomme kan inddeles i to hovedgrupper: Dem, der rammer nethindens stavceller, og dem, der rammer nethindens tapceller (se figur 1). Stavcellerne er meget lysfølsomme sanseceller, der sidder i den perifere del af nethinden. Stavcellerne bruges til at se med, når det er mørkt. Hvis de er syge, går det ud over nattesynet og det perifere syn. Hvis en patient med stavsygdom befinder sig udendørs efter mørkets frembrud, kan patienten kun se det skarpe lys fra gadelygterne. Alt andet henligger i mørke.

”Det er meget ubehageligt for patienterne, der risikerer at falde over kantsten eller ned i huller. Forældre til børn med stavsygdomme fortæller tit, hvordan deres børn altid efterlader en stribe af lys efter sig gennem huset, da de ikke kan gå fra et oplyst rum og ud i en mørk gang eller lignende. Jeg hører også ofte beretninger om børn, der løber ind i borde, banker hovedet ind i et skab eller falder over hunden,” fortæller Line Kessel.
Ved tapsygdom ser patienterne dårligt i dagslys, da tapcellerne kræver et højt niveau af lys for at fungere. Tapcellerne findes primært i nethindens gule plet (makula), hvor skarpsynet er lokaliseret. De bruges til at genkende farver og se detaljer. Patienter med tapsygdom har derfor svært ved at se farver og detaljer.
”Ved tapsygdom er nethinden konstant i en tilstand, som hvis du vågner midt om natten og ikke kan se farver og detaljer såsom ansigtstræk. Patienter med tapsygdom er ofte ekstremt lysfølsomme, og de har tendens til at fiksere blikket decentralt. Børnene leger under sofabordet for at undgå dagslys, og familierne bor for nedrullede gardiner, da børnene ikke kan holde dagslyset ud,” siger Line Kessel.
Ved stavsygdom vil det typisk være muligt at se forandringer på nethinden allerede tidligt i sygdomsforløbet, mens nethinden kan se normal ud i lang tid ved tapsygdom.
Luxturna er en genterapi, der i 2019 blev godkendt af både de amerikanske – og de europæiske lægemiddelmyndigheder. Luxturna er en engangsbehandling, der er godkendt til behandling af børn og voksne med synstab som følge af arvelig RPE65-relateret nethindesygdom. Luxturna sprøjtes ind under nethinden. Herved overføres arvemateriale, som koder for normalt RPE65-protein, til nethindens pigmentepitelceller. Luxturna gør de syge celler i stand til at danne normalt RPE65-protein, hvilket genopretter funktionen af nethindens fotoreceptorer. RPE65-genet er et lille gen, og derfor er det muligt at overføre genet via en uskadeliggjort viruspartikel.
Godkendelsesstudiet viste, at 90 pct. af de patienter, som blev behandlet med Luxturna, oplevede en bedring af synet efter et år, og 65 pct. kunne fejlfrit navigere igennem en labyrint med en rimelig hastighed ved lav belysning. Nogle af patienterne kunne for første gang i deres liv se snefnug og stjerner.
I 2019 afviste Medicinrådet at anbefale Luxturna som standardbehandling, da rådet vurderede, at prisen på lægemidlet var urimeligt høj.
Tidlig sygdomsdebut
Som oftest opdages arvelig nethindesygdom i barne- eller teenageårene eller i det tidlige voksenliv. Grundet arveligheden vil sygdommene i sjældne tilfælde være kendt fra fødslen, men det forholder sig langtfra altid sådan. Ydermere kan sygdommene opstå som følge af nyopståede genfejl.
”Diagnoserne stilles ofte først, når sygdommene er meget fremskredne – når skarpsynet eller synsfeltet er meget påvirket. Børn er gode til at finde måder at kompensere for deres nedsatte syn. Og hvordan skal et barn vide, at det ikke kan se stjerner på nattehimlen, hvis det aldrig har set stjerner før? Vi ser som regel først patienterne, når deres centrale eller perifere syn er markant nedsat,” siger Line Kessel.
Udredning for arvelig nethindesygdom foregår på hospitalet. Indledningsvis forholder øjenlægen sig til symptomer og måler synet ved en almindelig synstest for at undersøge, om tapcellerne er påvirkede. Herefter foretages en række fotografiske undersøgelser af øjnene samt en elektrofysiologisk analyse. Ved en elektrofysiologisk analyse sættes en ultratynd elektrode på øjet, som måler impulsmønsteret fra fotoreceptorerne i mørke og under relativ kraftig belysning. Herved er det muligt at identificere sygdom i henholdsvis stav- og tapcellerne.
”Nogle gange tager vi også en blodprøve, som analyseres for genfejl. Det gør vi i de tilfælde, hvor vi har interesse i at fastslå, hvilken variant af en sygdom der er tale om. Visse varianter er associeret med sygdom andre steder i kroppen, og det er vigtigt, at vi ved, om vi – ud over at holde øje med øjensymptomer – også skal have fokus på for eksempel kognitive symptomer eller symptomer fra nyrerne,” forklarer Line Kessel.
Genetiske analyser foretages ydermere, når informationer om sygdommens arvegang er relevante i forhold til at forudsige kommende børn og søskendes sygdomsrisiko. Det er langtfra altid, at den genetiske årsag til en arvelig nethindesygdom er kendt.
Nye genetiske behandlinger
En anden årsag til at undersøge generne er, at der de seneste 10-15 år har været meget fokus på udvikling af behandlinger målrettet bestemte genfejl, såkaldte genterapier. Genterapier er behandlinger af genetisk bestemte sygdomme, hvor der overføres arvemateriale til kroppens celler eller indsættes celler med raske gener som erstatning for eller supplement til celler med syge gener. Genterapier til behandling af arvelig nethindesygdom virker kun, hvis der stadig er stav- eller tapceller tilbage i nethinden.
Line Kessel har to ph.d.-studerende, der med støtte fra Øjenforeningen ser på arvelig nethindesygdom, Mette Kjøbæk Gundestrup Andersen og Kristian Lisbjerg.
Mette Kjøbæk Gundestrup Andersen projekt:
Karakterisering af danske patienter med tap- og tap-stav-dystrofi
Ph.d.-projektets hovedformål er at undersøge patienter med arvelige sygdomme i tapcellerne (akromatopsi) og tapdystrofi. Mere præcist foretages en detaljeret undersøgelse af sammenhængen mellem den genetiske baggrund og sygdommenes udtryk hos den enkelte patient, en kortlægning af sygdommenes ubehandlede forløb for at forbedre rådgivningen af fremtidige patienter samt en undersøgelse af behovet for optiske hjælpemidler til patientgruppen (specialoptik, filterbriller eller kontaktlinser). Denne viden er relevant, når der engang – om formentlig ikke så længe – kommer genterapi med akromatopsi.
Kontaktoplysninger: E-mail: mekjan02@regionh.dk, tlf.: 29 20 48 62
Kristian Lisbjergs projekt:
Sammenhæng mellem kliniske og genetiske forhold ved PRPF31-relateret RP
Ph.d.-projektet omhandler de tilfælde af den fremadskridende nethindesygdom Retinitis Pigmentosa (RP), der skyldes en dominant genfejl i PRPF31-genet. I projektet foretages omfattende øjenundersøgelser og gentest af patienterne for herved at kunne beskrive kliniske og genetiske karakteristika for gruppen. Resultaterne skal bruges til at klarlægge, hvorfor RP kun slår ud hos nogle af de personer, der har fejl i PRPF31-genet, samt hvilke genetiske faktorer der har betydning i denne sammenhæng. Denne viden vil være værdifuld i forbindelse med diagnostik, prognose og fremtidig forskning i sygdommen.
Kontaktoplysninger: E-mail: kristian.lisbjerg@regionh.dk, tlf.: 29 20 48 62
I 2019 kom genterapien Luxturna på markedet i USA og Europa. Det er en engangsbehandling til børn og voksne med den arvelige nethindesygdom, der hedder RPE65-relateret nethindesygdom eller Lebers Kongenitale Amaurose (LCA). Det er en langsomt fremadskridende sygdom, der over tid fører til blindhed. Sygdommen er uhyre sjælden og rammer globalt set én ud af en million mennesker. I Danmark er forekomsten lidt hyppigere med 30 patienter på landsplan. Før Luxturna var der ikke helbredende behandling mod RPE65-relateret arvelig nethindesygdom. Luxturna gør de syge celler i stand til at danne normalt RPE65-protein, hvilket genopretter funktionen af nethindens fotoreceptorer.
”Vi kender endnu ikke langtidseffekterne af Luxturna, men indtil videre ser det ud til, at behandlingen gør en kæmpestor forskel for synet og livskvaliteten. Nethinden bliver ikke fuldt fungerende, men behandlingen gør, at patienterne bliver selvhjulpne. De kan finde hen til deres uddannelsesinstitution, de kan bestride et job, og de kan navigere i mørke. Det er meget rørende at se videoer af børn, der pludselig bliver i stand til at se og opfatte den verden, der hidtil har været skjult for dem,” siger Line Kessel.
Medicinrådet afviste imidlertid at tage Luxturna i brug som standardbehandling herhjemme, da rådet mente, at behandlingens pris var urimelig høj. Det danske pristilbud for behandlingen er ikke kendt af offentligheden, men i USA er listeprisen 850.000 dollar svarende til 5,6 mio. danske kroner. Listeprisen er imidlertid ikke identisk med den pris, produktet ender med at få. Traditionelt set er danske priser lavere end amerikanske.
”Genterapier er rettet mod én bestemt genfejl, som ofte kun optræder hos ganske få patienter. Når medicin er så personlig, er den meget dyr at udvikle og afprøve, hvilket betyder, at prisen per behandling bliver meget høj – sådan som det er tilfældet med Luxturna. Min vurdering er, at Luxturna vil gøre en væsentlig forskel for patienterne! Vi taler om patienter, som ellers bliver blinde,” fastslår Line Kessel.
Andre behandlinger på vej
Genterapi er den nye behandlingsform, som der er størst tiltro til og mest opmærksomhed omkring for tiden. Og mange medicinalfirmaer har genterapier mod andre typer af arvelig nethindesygdom end lige RPE65 i pipelinen. Line Kessel forudser, at de næste genterapier, der kommer på markedet, vil være rettet imod akromatopsi, X-bunden Retinitis Pigmentosa og choroideremi.

Genterapier er imidlertid ikke den eneste nye behandlingsform, der er under udvikling. Et andet område, der har øjenforskningens interesse, er stamceller. Stamceller er celler, der endnu ikke er specialiseret til at have bestemte egenskaber, og tanken bag stamcellebehandling er, at de umodne celler kan erstatte de syge celler, der er gået til grunde. Der forskes især i stamcellebehandling i forhold til øjensygdommene AMD og Stargardt.
”Lige nu er forskningen der, hvor forskerne er i stand til at få stamcellerne til at overleve i nethinden. Men at få dem til at integrere sig, blive funktionelle og undgå uønsket vækst, det er straks en anden og mere kompleks sag. Der arbejdes intenst, men vi er langtfra lige så langt fremme som med genterapi,” siger Line Kessel.
Foruden stamcelleterapi forskes der i at udvikle implantater, der kan indopereres i nethinden og genetablere signalvejen fra nethinden til hjernen. Og der er projekter i gang, hvor disse signalveje forsøges etableret uden om øjet. Endelig forskes der også i såkaldt optogenetisk terapi, hvor forskerne forsøger at manipulere celler i nethinden til at blive lysfølsomme, således at disse celler kan erstatte de syge fotoreceptorer.
”Det er et vanvittig spændende tidspunkt at være øjenlæge med alle de nye behandlinger, der er på vej. Jeg har tiltro til, at prisen på genterapierne inden alt for længe sænkes til et niveau, hvor det er realistisk, at også de danske myndigheder giver grønt lys til, at vi kan behandle de patienter, der har så meget brug for det. Jeg tror på, at fremtiden er lys – bogstavelig talt,” slutter Line Kessel.
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.







