Fremtidens behandling af AMD og andre arvebetonede øjensygdomme
Genetiske øjensygdomme udgør en meget stor del af de svære, ubehandlelige øjensygdomme. Den seneste forskning viser, at nye attraktive behandlinger kan blive tilgængelige indenfor få år. En grundig og målrettet forberedelse kan sikre, at disse behandlinger i tide når frem til danske patienter med genetisk betingede øjensygdomme

Foto: iStock.com/Raycat
Genetisk betingede øjensygdomme opstår på grund af sygelige ændringer i bestemte gener.
I den klassiske arvelighedslære blev sygdommene identificeret udfra deres familiære optræden og arvegangen blev i mange tilfælde klarlagt. En række sjældne, men alvorlige sygdomme, som rammer nethinde og synsnerve, ofte med svært synstab eller blindhed til følge, er kendte, men desværre, indtil nu, uhelbredelige.
Man har i mange år vidst, at en del øjensygdomme havde en familiær disposition og efter at det er blevet muligt at kortlægge de menneskelige gener, har man opdaget, at nogle af de almindelige øjensygdomme optræder langt hyppigere hos personer med bestemte gener. Fx kan grå stær og AMD for henholdsvis halvdelen og tre fjerdeles vedkommende tilskrives tilstedeværelsen af særlige gener.
Selv om man har fundet et defekt gen, er det ofte en vanskelig proces at identificere de vævskader, som dette defekte gen fremkalder og årsagerne hertil. Disse processer må klarlægges i detaljer, før det er muligt at udvikle virkningsfulde behandlingsmetoder.
Der tegner sig flere muligheder for, at man i fremtiden kan behandle de genetiske øjensygdomme, som i dag er uhelbredelige.
De hyppigste alvorlige arvelige øjensygdomme udspiller sig i nethinden
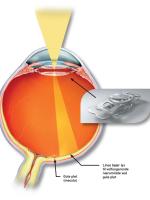
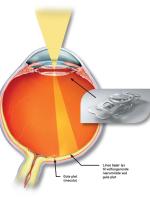
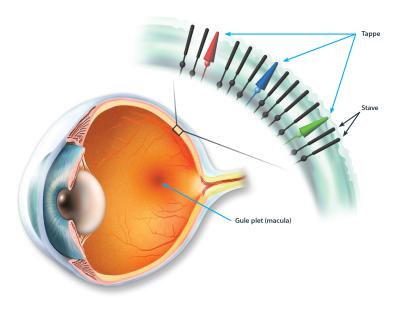
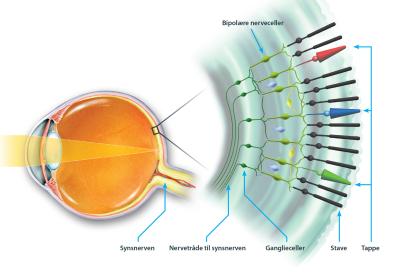
Nethinden beklæder øjets inderside og indeholder blandt andet dagslysceller (tappe) - som er nødvendige for detaljesynet og farvesynet - og natlysceller (stave) (Fig. 1).
Stavene og tappene er gensidigt afhængige af hinanden, idet de udveksler signalmolekyler, som er nødvendige for at opretholde normal funktion. Ved øjensygdommen retinitis pigmentosa - der er uhelbredelig og meget ofte fører til blindhed - er der en genetisk defekt i stavene, som bevirker, at disse sanseceller - og dermed nattesynet - går tabt. Derved går også de for tappene livsnødvendige signalmolekyler tabt, således at patienterne på langt sigt også bliver dagblinde og dermed helt blinde, til trods for, at der ikke er nogen genetisk defekt i tappene.
Det er lykkedes at identificere nogle af de involverede signalmolekyler, hvilket giver håb om, at de kan fremstilles kunstigt og tilføres som et lægemiddel, fx ved indsprøjtning i øjets glaslegeme. Behandlingen er under udvikling, og hvis alt går vel, vil den blive forsøgt anvendt på patienter med retinitis pigmentosa inden for de nærmeste fem år.
Anvendelse af et bestemt enzym synes at have virkning på Stargardts øjensygdom
Når lys rammer nethindens sanseceller (stave og tappe) startes en kompliceret biokemisk proces, som resulterer i afsendelse af et elektrisk signal til hjernen, hvor det fører til en synsoplevelse.
Ved Stargardts øjensygdom er der en genetisk defekt, som bevirker, at den biokemiske proces, som løbende finder sted i forbindelse med lyspåvirkning, resulterer i ophobning af affaldsstoffer i sansecellerne. Dette medfører, at disse efterhånden dør, således at synsfunktionen nedsættes - ofte allerede i barndommen. Den genetiske defekt rammer et enzym, som medvirker ved omdannelsen af vitamin A til synsfarvestof. Når enzymet ikke virker, bliver der ophobet skadelige mellemprodukter i omdannelsen af vitamin A.
Stargardts sygdom findes også hos dyr, som man med held har behandlet med vitamin A-lignende lægemidler, som hæmmer ophobningen af skadelige mellemprodukter i dannelsen af synsfarvestoffet.
De første spæde forsøg på mennesker er indtil videre forløbet gunstigt, og det forventes, at forsøg i stor skala vil blive iværksat indenfor fem år.
Tilførsel af lægemiddel, som kompenserer for arvelig stofskiftefejl
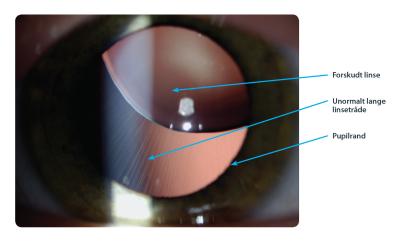
Patienter med Marfans sygdom har abnormt bindevæv. Dette kan resultere i, at øjets linse bliver løs, således at den glider væk fra pupillen, hvilket giver anledning til synsnedsættelse
(Fig. 2). Det er velkendt, at Marfans sygdom fører til udspiling af den store legemspulsåre (aorta-aneurisme), som kan briste med dødelig udgang. Opdages sygdommen i tide, kan aorta-aneurismet dog behandles operativt.
Sygdommen skyldes en defekt i et gen, som koder for et bindevævsprotein. Proteinet binder og regulerer dermed en vækstfaktor, som igen regulerer dannelsen af bindevæv.Derfor findes vækstfaktoren frit i bindevævet i for høj koncentration, hvilket medfører dannelsen af et abnormt slapt og eftergiveligt bindevæv.
Da man først forstod, at et for højt vækstfaktorsignal er med til at fremkalde sygdom, så man sig om efter kendte lægemidler, som hæmmer signalet af vækstfaktoren. Det fandt man i form af et velkendt middel til behandling af blodtryksforhøjelse. Derfor foregår der nu forsøg, hvor lægemidlet losartan søges anvendt til at eliminere behovet for operation i brysthulen af patienter med Marfans sygdom. Dette eksempel viser, hvor vigtigt det er, ikke blot at finde et sygdomsgen, men også at foretage en grundig udforskning af den måde, hvorpå den genetiske fejl fører til sygdom.
Nye muligheder for forebyggelse af AMD i horisonten
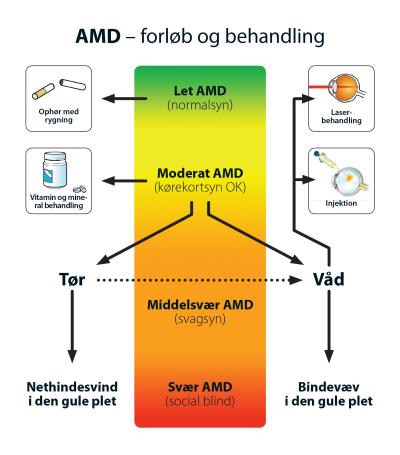
Alderspletter på nethinden (aldersrelateret maculadegeneration, AMD) udvikler sig over mange år fra let til svær AMD (Fig. 3).
Selv om sygdommens sene og svære former i nogen grad kan forebygges og behandles, savnes fortsat metoder til en egentlig behandling af grundsygdommen, dvs. den lette til moderate tørre AMD.
Vores immunforsvar har længe været mistænkt for at medvirke til at forårsage AMD, men det var alligevel en overraskelse, da man i 2005 kunne bevise, at mere end halvdelen af forekomsten af AMD kan forklares udfra nogle variationer i menneskets komplementsystem, som er den ældste del af vort immunforsvar. Derfor forsøger man nu at udvikle lægemidler, som kan hæmme komplementsystemet og derved eliminere tør AMD, hvilket også må forventes at fjerne våd AMD, som er en komplikation til tør AMD.
Genterapi kan være vejen til forebyggelse af AMD, diabetisk nethindesygdom og Lebers nethindeblindhed
Det blev tidligere i år meddelt, at det nu er lykkedes kunstigt at tilføre et manglende gen til patienter med en særlig sjælden variant af medfødt nethindeblindhed (LCA). Denne sygdom giver anledning til svær synsnedsættelse tidligt i livet. Den variant af LCA, som man behandlede, har den særlige egenskab, at cellerne i nethinden forbliver i live i mange år, selv om den aldrig har fungeret.
Ved at tilføre det manglende gen kunne man vække de slumrende celler og få dem til at fungere på ny. Synsforbedringen var meget beskeden, men det skyldes formentlig, at man til forsøget havde udvalgt patienter, som ikke havde meget at miste, hvis forsøget skulle gå galt, og som var voksne og selv kunne tage stilling til forsøget. Da disse patienter ikke har haft normalt syn fra den tidlige barnealder, er synscentret i deres hjerne heller ikke udviklet normalt, hvilket begrænser udbyttet af behandlingen. Efterhånden vil man, hvis alt går godt, arbejde sig frem til at behandle børn under fem år, hvor det største potentiale for synsgevinst findes.
En anden og enklere form for genterapi består i at indgive særlige små genstykker (RNA-molekyler), som kan slukke for produktionen af uønskede stoffer. Dette princip, RNA-interferens, er under afprøvning til behandling af nethindesygdommene diabetisk retinopati og AMD - alderspletter på nethinden - blandt andet i Glostrup, hvor det nye campus omfatter både Glostrup Hospitals Øjenafdeling og Kennedy Centret.
Tilførsel af stamceller kan blive flere uhelbredelige øjensygdommes endeligt
Mange nethindesygdomme medfører kun tab af nethindens sanseceller, hvorimod de nerveceller og nervetråde, som transporterer sanseindtrykket til hjernen, fortsat fungerer (Fig. 4).
Det gælder fx retinitis pigmentosa. Man forsøger derfor at reparere nethinden ved at tilføre stamceller, som, efter indsprøjtning i rummet bag nethinden, kan udvikle sig til nye sanseceller. Disse celler er, håber man, selv i stand til at finde ud af, hvordan de skal skabe en forbindelse til nethindens nerveceller og derved genoprette synsfunktionen.
Man kan forestille sig, at stamcellerne fx udtages fra patientens egen knoglemarv, hvorefter de opformeres i et laboratorium, før de indgives i øjet. Undervejs skal cellerne stimuleres med forskellige midler, således at de opdrages til at opføre sig som spæde nethindeceller. Det er endnu ikke lykkedes at få styr på opdragelsen, men forskningen er løfterig, fordi man kan se, at cellerne undertiden kun behøver så at sige at blive peget i den rigtige retning, hvorefter de selv, i kraft af deres stamcelleegenskaber, vil finde vej til det ønskede resultat. Et gennembrud i forskningen kan give mulighed for forsøg på mennesker indenfor de nærmeste 5-10 år. Glostrup Hospital foretager forsøg med stamcellebehandling i øjet.
Synsprotese til erstatning for nethinden eller hele øjet er mere end fantasi
Det er påvist, at man kan stimulere nethinden med svage elektriske strømme på en sådan måde, at en ellers blind patient vil opleve at se lys.
De teknologiske muligheder, som moderne elektronik giver, kan i princippet anvendes til at fremstille en nethindeprotese bestående af et kamera, en computer og en elektrode, som giver nethinden små stød i et sådant mønster, at patienten ser gennem kameraet og får et brugbart syn. Der er et stort udviklingsarbejde i gang for at fremstille elektronikken tilstrækkelig kompakt, optimalt programmeret og uden vævsafstødning, så proteserne kan anvendes i praksis. Behandlingen vil i første omgang være et tilbud til patienter, som er helt blinde, hvorimod patienter med et brugbart restsyn vil være bedre tjent med at opøve sig i brugen af dette. Det forventes, at der vil gå 5-10 år, før behandlingen kommer i brug.
Det giver anledning til optimisme, at man har haft meget stor succes med en tilsvarende, men enklere protese til behandling af døvhed (cochleaimplantat i det indre øre), blandt andet hos patienter med Ushers sygdom (retinitis pigmentosa) samtidig med arvelig døvhed. Man forsøger også at udvikle proteser, som sender signalet direkte ind i hjernen på patienter, som ikke har noget væv tilbage i nethinden eller i det indre øre.
Hvordan kan danske øjenafdelinger bidrage til udvikling af ny behandling af arvelig øjensygdom?
Det er nødvendigt, at man i Danmark forbereder indførelsen af nye behandlinger af arvelig øjensygdom, specielt for de patienter, som i dag slet ikke kan behandles.
Disse patienter har i øjeblikket deres primære øjenlægekontakt i rehabiliteringssystemet, dvs. på Kennedy Centret samt hos regionernes synscentraler, synskonsulenter, synspædagoger, osv.
Det er en vigtig opgave for dette netværk og for landets øjenafdelinger at foretage en præcis kortlægning af de omtalte sygdommes forekomst, således at patienterne er kendt og kan tilbydes behandling i den takt, den bliver tilgængelig.
Forberedelse af indførelsen af en sådan behandling kræver på forhånd en præcis diagnose for hver enkelt patient, inklusive bestemmelse af den sygdomsfremkaldende genændring. Sådan præcis diagnostik foreligger for nærværende kun for et mindretal af patienterne, idet man generelt og med nogen rimelighed sparer på udgifterne til detaljeret diagnostik af uhelbredelige tilstande. Det er imidlertid klart, at man med så mange behandlingsmuligheder i sigte må sadle om og i god tid foretage en molekylærgenetisk udredning af alle patienter.
Det er også indlysende nødvendigt at finde sygdomsramte børn og unge voksne, før de udvikler symptomer, idet mange behandlinger skal iværksættes, inden patienten opdager sine synsproblemer. Det er man hidtil veget tilbage for, af frygt for unødigt at sygeliggøre patienterne. Det gælder dog, at patienterne, når de får diagnosen, ofte giver udtryk for, at de gerne ville have haft diagnose tidligere, så de kunne have sparet dem for bryderier, misforståelser og mobning.
Velfungerende netværk mellem forskere og patienter, kendskab til sygdommenes spontane udvikling samt tilgængelighed af metoder til kortlægning af nethindens struktur og funktion er nødvendige for at opbygge de nødvendige kompetencer og arbejdsgange.
Kennedy Centret i Glostrup er et landsdækkende behandlings- og forskningscenter, som udfører diagnostik af arvelig øjensygdom og mental retardering, rehabilitering af personer med synsnedsættelse og klinisk genetisk rådgivning. Kennedy Centrets opgave er at finde patienterne med de svære arvelige øjensygdomme, helst tidligt og helst alle, at stille en præcis klinisk diagnose og at monitorere og udforske øjensygdommene. Kennedy Centrets landsdækkende DNA Bank for arvelige øjensygdomme samler prøver fra hele landet og opbevarer prøverne vederlagsfrit, også for eksterne forskere. Sammen med Glostrup Hospital, som er nabo på campusområdet i Glostrup, og Københavns Universitet, forberedes hjemtagelsen af nye behandlingsmetoder for arvelig øjensygdom, både gennem basalvidenskabelige studier og behandlingsstudier.
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.