Hvordan kan vi genskabe tabt syn?

Foto:
18percentgrey / Shutterstock.com
Øjenspecialet har gennem de sidste 50 år udviklet sig dramatisk
Man kan lege med tanken om, at en professor ved øjenafdelingen på Rigshospitalet i 1965, fik lov til at gå en tur på øjenafdelingen ved Rigshospitalet/Glostrup Hospital i dag. Han ville se, at den mikrokirurgiske teknik har udviklet sig, så vi nu rutinemæssigt, sikkert og i høj grad ambulant, leverer titusindvis af grå stær operationer, operationer for nethindeløsning, diabetisk nethindesygdom, grøn stær og endnu flere øjensygdomme, som ikke - eller kun vanskeligt - kunne behandles i hans tid. Han ville se laserbehandling anvendt for en hel buket af nethindesygdomme. Især inden for det sidste tiår er der sket så at sige en revolution inden for behandlingen af aldersrelateret makula degeneration (AMD) og en række andre nethindesygdomme.
Faldende tilfælde af blindhed skyldes effektiv medicinsk behandling
Undersøgelser af den vestlige verdens aldrende befolkninger, herunder den danske, har vist en entydigt nedadgående tendens i forekomsten af blindhed og svagsyn. (Fig. 1) I det sidste tiår har man set, at faldet i blindhed er korreleret med indførelsen af effektiv behandling af AMD ved injektion i øjet med væksthæmmende medicin (intravitreal anti-VEGF behandling).
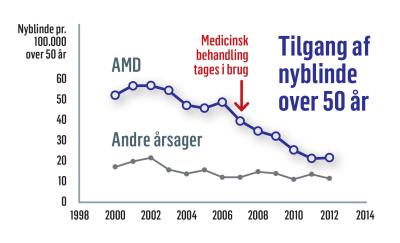
I dag er sygdomme i nethinden og synsnerven dog fortsat de altdominerende årsager til blindhed i Danmark. AMD er den væsentligste årsag i den ældre aldersgruppe, mens arvelige nethindesygdomme er den væsentligste årsag til ’blindeår’ i befolkningen. Grøn stær og andre synsnervesygdomme er årsag til ca. 20% af blindhed i DK (data fra undersøgelser udført af bl.a. Helena Buch og Tracy Høegh støttet af Øjenforeningen).
Vigtigste årsag til svært synstab er ophør af nethindens cellefunktioner
Langt den væsentligste sygdomsmekanisme bag blindhed i Danmark og i den øvrige vestlige verden er tab af celler i nethinden. En del af den nuværende forskningsindsats handler derfor om at forstå sygdommene bedre for derved at kunne raffinere og udvikle behandlinger, der forhindrer cellerne i at dø, og/eller forbedrer funktionen af næsten døde celler, fx ved at tilføre raske gener, diverse stofskifteprodukter eller vækstfaktorer. Resten af denne artikel handler om den anden hovedstrøm i forskningen, nemlig, hvordan vi kan genskabe funktion i nethinder, hvor funktionen er tabt på grund af celledød.
Elektroniske nethinde-proteser er en teknisk udfordring
Inden for ørespecialet har indførelsen af elektroniske proteser (cochlear implantater), genskabt hørelsen hos en række døve patienter. Den optimisme, som disse implantaters succes har skabt, er ikke indfriet i øjenspecialet. Det er betydeligt vanskeligere rent teknisk at lave en elektronisk nethindeprotese. Der er dog to godkendte nethindeproteser på markedet (amerikanske ARGUS-2 og tyske Retinal-Implant, se VOS 2014/4). Der er på verdensplan implanteret knap et par hundrede af disse proteser. De giver kun et meget groft syn, og et meget begrænset synsfelt i de tilfælde, hvor proteserne er i funktion. Kun få af patienterne har protesen tændt uden for deres kliniske træningssessioner, så det er kun et lille mindretal af patienter med implantater, som føler, at de har gavn af proteserne i disses nuværende udviklingsstade.
Genetisk manipulation af synsnerveceller kan genskabe lysfølsomhed
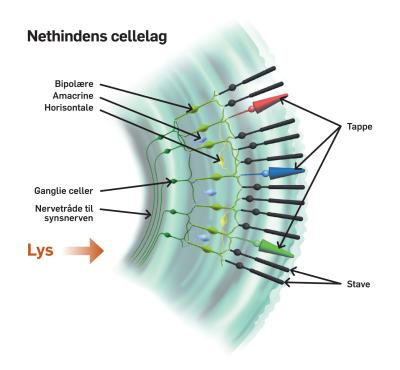
En anden mulighed er, gennem genetisk manipulation af de overlevende ganglieceller (Fig. 2), at gøre disse lysfølsomme. Denne såkaldte optogenetiske tilgang blev foreslået som metode til aktivering af nerveceller af Francis Crick i 1999 (Francis Crick fik Nobel-prisen for sin del af opdagelsen af den dobbelte DNA helix, en af de væsentligste opdagelser i forrige århundrede; han foreslog optogenetikken som 83-årig). Optogenetik er med held benyttet til at genskabe syn hos blinde mus, og feltet er under hastig udvikling.
Transplantation af nethindeceller har ikke hidtil været en farbar vej
Transplantation af celler og væv til behandling af funktionstab er velkendte behandlings-metoder i lægekunsten - også i oftalmologien - hvor transplantation af hornhinder, dele af hornhinder og såkaldte limbale stamceller er velkendt. Problemerne ved transplantation er også velkendte i form af varierende kvalitet af det transplanterede materiale og immunologiske afstødningsreaktioner.
Transplantation af nethindeceller som behandling af nethindesygdomme er en gammel drøm, som vi og andre forskere har arbejdet med i mange år. Nethinden har imidlertid en meget kompleks struktur, hvor cellerne interagerer med hinanden på en meget velorganiseret måde. Det er derfor et problem at få de transplanterede celler til at overleve og til at organisere sig i værtsnethinden på en sådan måde, at transplantationen resulterer i forbedret funktion. Yderligere problemer er kvaliteten af de transplanterede celler og immunologiske afstødningsreaktioner.
Ny stamcelleteknologi åbner døren på klem til opnåelse af synsforbedring
Moderne stamcelleteknologi giver mulighed for donormateriale af væsentligt forbedret kvalitet og har derfor skabt fornyet håb for, at celletransplantation kan anvendes til at erstatte nethindeceller, der er gået til grunde.
Der findes forskellige typer af stamceller:
Totipotente stamceller
Totipotente stamceller er stamceller, der kan dele sig stort set uendeligt, og som kan blive til alle typer af væv. Totipotente stamceller er den befrugtede ægcelle, den såkaldte zygote (Fig. 3), og de celler, der opstår som følge af de første få celledelinger efter zygoten.
Pluripotente/embryonale stamceller
Pluripotente stamceller har også stort set uendeligt delingspotentiale, som kan udvikle sig til en række forskellige celletyper (celler fra alle fosterets tre kimblade, men ikke moderkagen), dog uden at være totipotente. Pluripotente stamceller, kaldes også embryonale stamceller, og udgøres af den indre cellemasse i et 5 dage gammelt foster (den såkaldte blastocyst). Ved hjælp af pluripotente stamceller kan man i laboratoriet skabe store mængder af en række forskellige celletyper ved en kontrolleret proces, så cellerne er relativt ensartede. Man kan yderligere genetisk modificere cellerne, så eventuelle gendefekter rettes. Man kan også ændre cellerne, så de bliver mindre immunogene, og derfor mindre tilbøjelige til at blive afstødt.
Progenitorceller
Der er åbenlyse etiske problemer ved at anvendte embryonale stamceller fra mennesker. Stamceller med mere begrænset potentiale kan opnås fra moderkager, aborterede fostre samt fra knoglemarv og andre væv i udvoksede individer. Disse såkaldte begrænset pluripotente stamceller, eller progenitorceller, kan kun ekspanderes i begrænset omfang, og de kan kun udvikle sig til et begrænset antal væv. Der kører rundt omkring i verden en række forsøg med embryonale stamceller og progenitorceller til behandling af forskellige nethindesygdomme. Vi har i samarbejde med forskere fra Harvard Medical School arbejdet med transplantation af progenitorcellederiverede sanseceller til svin. Disse forsøg har ført til, at fase I studier på patienter med arvelige nethindesygdomme er ved at blive igangsat i USA.
IPSC (inducerede pluripotente stamceller)
For knap 10 år siden fandt den japanske forsker Shinya Yamananka en metode til at få færdigudviklede celler til at ’gå baglæns’ i deres udvikling og blive til pluripotente stamceller, en opdagelse, der allerede i 2002 resulterede i, at Yamananka, kun 50 år gammel, modtog Nobelprisen i medicin. I den sidste dekade har der været en eksplosiv interesse for disse såkaldt inducerede pluripotente stamceller (IPSC). Det er således muligt fra en almindelig hudbiopsi fra en patient, at skabe IPSC, som immunologisk er identiske med patientens øvrige celler. Disse kan efterfølgende drives til at udvikle sig til stort set alle celletyper, og derved har man fået et hidtil uset kraftfuldt redskab til at studere fx effekten af genetiske defekter på forskellige væv i laboratoriet. IPSC teknologien giver også mulighed for, hos fx patienter med arvelige nethindesygdomme, at udtage en hudbiopsi, derfra skabe IPSC, og dernæst med moderne genteknologi korrigere gendefekten, og derved skabe raske sanseceller, som kan transplanteres til patienten. IPSC har den fordel fremfor embryonale stamceller og progenitorceller, at cellerne immunologisk ligner værtens egne celler og derfor (teoretisk) ikke vil blive afstødt efter transplantation. Der kører forsøg med IPSC deriverede sanseceller og pigmentepithel-celler ved flere etablerede institutioner.
Stamcellernes evne til at udvikle sig til en række væv er et tveægget sværd
I nogle forsøg med stamceller har man set, at stamcellerne har udviklet sig til svulster. Dette er mere udtalt jo mere pluripotente cellerne er og er måske et særligt problem for IPSC. Det er måske ikke så overraskende, fordi de celler, der danner svulster, er umodne ligesom stamcellerne. Den oprindelige metode til produktion af IPSC involverede aktivering af kraftige onkogener, d.v.s. gener der får celler til at udvikle svulster. Nyere protokoller undgår anvendelsen af disse onkogener. Stamcelleterapi er derfor ikke en risikofri behandling, og bør i øjeblikket ikke foregå uden for kontrollerede forsøg. Desværre udbydes disse behandlinger på nettet til en række sygdomme af mindre seriøse klinikker i en række ikke EU-lande.
’Tissue-engineering’
Som ovenfor nævnt er behandling af nethindesygdomme med celletransplantation vanskeliggjort af, at de transplanterede celler skal inkorporeres i nethindens komplekse struktur. Man kan prøve at løse disse problemer ved at indføre grupper af celler støttet af forskelligt materiale, så man allerede i laboratoriet prøver at genskabe det tabte væv. Denne tilgang kaldes vævs-ingeniør-kunst (engelsk: tissue-engineering). Vi har arbejdet en del med dette i forbindelse med vore forsøg på at transplantere pigmentepithelceller som behandling af AMD.
Aktuelle stamcelle forsøg i Danmark
På Københavns Universitet har vi i mange år arbejdet med transplantation af pigmentepithelceller (Fig.2) i dyremodeller, og i øjeblikket arbejder vi i samarbejde med amerikanske forskere med retinale progenitorceller, ligesom vi er ved at igangsætte et forsøg med transplantation af ganglieceller med de samme samarbejdspartnere.
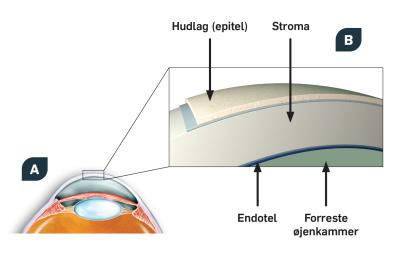
I tæt samarbejde med hornhindeforskere på Aarhus Universitet er vi ved at igangsætte et nationalt projekt, der skal kunne etablere et stamcellebaseret indre cellelag i hornhinder (endotel) til transplantation (Fig. 4).
I hvert skridt har Øjenforeningen ydet uvurderlig økonomisk støtte til vores forskning.
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.







