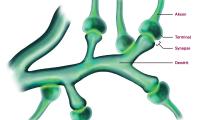
Kjers sygdom – arvelig synsnerveskrumpning (ADOA - Autosomal Dominant Opticus Atrofi)
Et studie der søger at påvise årsager til og behandling af denne hidtil uhelbredelige øjensygdom
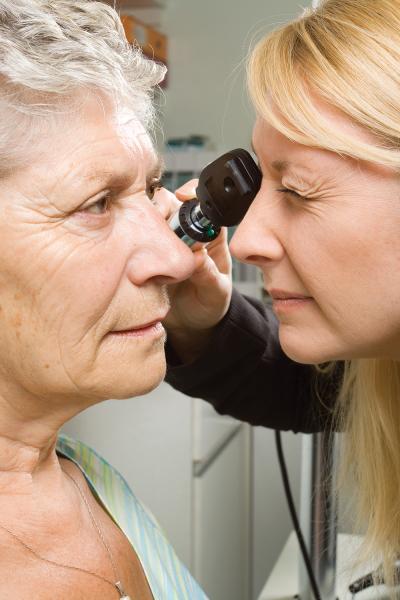
Kjers dominante opticus atrofi, også kaldet autosomal dominant opticus atrofi (ADOA), er en relativ hyppig arvelig øjensygdom og den hyppigste form for medfødt synsnervelidelse i Danmark. Sygdommens arvegang er dominant, hvilket indebærer – i modsætning til de vigende arvelige sygdomme - at der ofte ses sygdom i flere generationer. Der er ved hver undfangelse 50 % sandsynlighed for, at anlægget gives videre. Der er stor variation i såvel sygdomstegn som gennemslagskraften af arveanlægget, hvorfor der indenfor samme familie kan være nogle med svær synsnedsættelse og andre med næsten normalt syn blandt de, der bærer arveanlægget.
Det gen (arveanlæg), der er ansvarligt for ADOA, hedder OPA1. Det er mutationer (genændringer) i OPA1, der fremkalder sygdommen. Den samme mutation kan give forskellig grad af synsnedsættelse indenfor samme familie. Der må altså være andre faktorer end mutationer i OPA1, der spiller en rolle i sygdomsudviklingen af ADOA. Det kan for eksempel være miljømæssige eller genetiske faktorer, som påvirker synsnerven under graviditeten og senere i livet.
Dette er baggrunden for, at man i dette studie vil kortlægge såvel mutationstyperne i OPA1 hos patienter med ADOA og forsøge at identificere nye gener og miljøfaktorer, som kan tænkes at påvirke forløbet af ADOA.
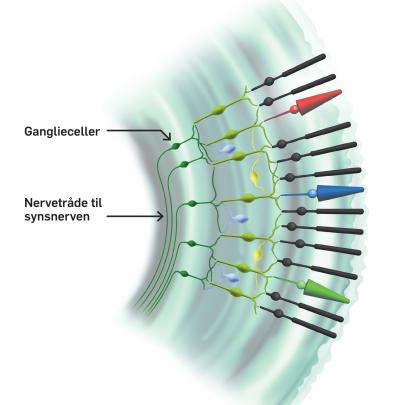
ADOA fører til langsomt tab af celler i nethinden, overvejende i det område, hvor skarpsynet dannes (macula) og de celler, som tabes, er gangliecellerne og deres udløbere (nervefibre) i synsnerven (Fig. 1).
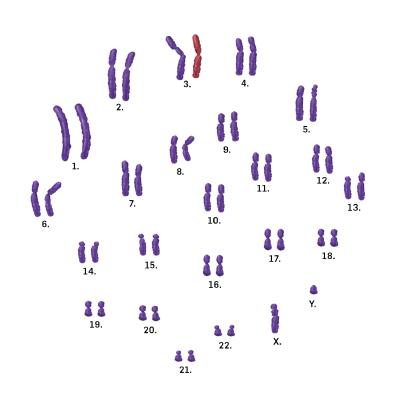
I Danmark rammes 1 ud af 10.000 af ADOA. I andre lande er hyppigheden lavere, nemlig 1 ud af 50.000. Det hænger sammen med, at der i Danmark findes mindst en founder mutation, dvs. en gammel genetisk fejl, som stammer fra en fælles forfader. Denne ene mutation i OPA1 genet er årsag til ADOA hos 42% af de danske patienter, der hidtil er undersøgt. OPA1 genet er for nærværende det eneste gen, hvor mutationer har vist at være årsag til ADOA. OPA1 genet sidder på den lange arm af kromosom nr. 3 (Fig. 2).
- Arves med 50% risiko fra den forælder, der har sygdommen
- Forekommer hos ca. 500 danskere
- Symptomdebut: Fra 4-6 års alderen
- Synsfeltdefekter: Primært centralt så læsesynet påvirkes
- Synet: Synsnedsættelse til evt. blindhed
- Farvesynsdefekter: Blå-gul (mest almindeligt). Rød-grøn
Sygdommens udvikling
De første symptomer kan ses mellem 4- og 6-årsalderen, men der er stor forskel mellem de sygdomsramte. Personer med milde tilfælde kan således forblive uden symptomer indtil tidlig voksenalder.
Synsfeltsdefekt
Der ses varierende grader af synsfeltdefekter ved ADOA. Synsfeltet er den del af omverdenen, man kan se uden at flytte blikket. Synsfelt danner normalt omtrent en cirkel, som det ses på Fig. 3. Den lille sorte plet angiver en naturlig (fysiologisk) blind plet på begge øjne. Den store sorte plet angiver en synsfeltsdefekt, der primært befinder sig i den del af nethinden, hvor skarpsynet dannes, det der anvendes, når man fx læser.

Synsnedsættelse
Synsstyrken – som ikke må forveksles med brillestyrken – er udtryk for øjets evne til at skelne små detaljer. Man kan beskrive normal synsstyrke ved at forestille sig, at man ser to stuefluer siddende seks meter borte på en hvid væg med en indbyrdes afstand på en fluebredde. Har man normal synsstyrke, vil man lige akkurat kunne se, at der er to fluer. Denne synsstyrke kaldes 1,0. Har man nedsat synsstyrke, vil man se de to fluer som én enkelt sort plet på væggen. Svær synsnedsættelse svarer til, at fluerne skal være 10 gange længere og bredere for, at man kan se dem. Denne synsstyrke kaldes 0,1. De fleste patienter med ADOA ser 0,1 eller dårligere på begge øjne, fra de er 40 år gamle.
Farvesynsdefekter
Patienter med ADOA har ofte svært ved at skelne blåt fra gult. De kan også have problemer med at skelne rødt fra grønt. Nedenfor ses et eksempel på en rød-grøn test (Fig. 4). Mennesker med normalt farvesyn kan se et 5 tal, men farveblinde ser et andet tal eller intet tal.

Projektet
Det overordnede formål med forskningsprojektet er at finde de endnu ukendte gener og miljøfaktorer, som fremkalder ADOA eller påvirker sygdommens sværhedsgrad. Det er vigtige forudsætninger for eventuelt at kunne udvikle en behandling af ADOA.
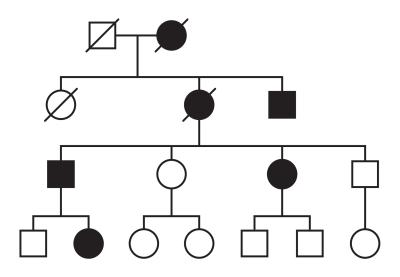
Dansk Familiearkiv for Arvelige Øjensygdomme på Kennedy Centret indeholder oplysninger om de fleste danske familier med ADOA. Fig. 5 illustrerer et stamtræ fra en typisk ADOA familie, hvor de sorte markører viser patienter med ADOA og hvide markører, at man ikke har sygdommen. Firkanter er mænd og cirkler er kvinder.
For at opklare de genetiske sammenhænge bag ADOA undersøger man syn og blodprøver både fra raske og syge familiemedlemmer. I første omgang har vi foretaget en udvidet søgning efter ændringer i OPA1, hvor alle kodende dele af genet er blevet kigget efter. Derefter har vi set efter mangel på store stykker af eller hele OPA1 genet. Vi fandt, at 10 ud af 100 familier manglede hele OPA1 eller store dele heraf. Dette forklarer den genetiske årsag til ADOA i disse familer.
I næste omgang vil vi se på oplysninger fra spørgeskemaer for at lede efter miljøfaktorer, som har betydning for sygdommens sværhedsgrad. Dernæst vil vi undersøge andre dele af patienternes samlede arvemasse, det såkaldte genom, for at finde gener, der kan forårsage ADOA. Vi vil gøre dette med en helt ny metode, hvor man i løbet af få dage kan aflæse alle de 20-25.000 gener hos et individ i samme analyse. Dette er muliggjort af information fra det Humane Genomprojekt, som kortlagde hele menneskets genom og nye højteknologiske maskiner. Det er ikke tidligere gjort på materiale fra patienter med ADOA.
Perspektiver
For at projektet kan lykkes, kræves for det første, at man udfører en nøjagtig undersøgelse af øjet hos raske og syge familiemedlemmer med de nyeste og mest nøjagtige metoder, der findes. Dette kaldes fænotypning. Derefter skal man gennemsøge forsøgsdeltagernes DNA og finde de koder, som bestemmer, om personerne har ADOA. Dette kaldes genotypning.
Øjenundersøgelsen vil sammenholdt med de genetiske data og data fra spørgeskema om miljøfaktorer bidrage til en forbedret klinisk klassifikation og ny viden vedrørende det sammensatte og varierende sygdomsbillede. En genetisk analyse kan af- eller bekræfte en mutations tilstedeværelse og en præcis genetisk vejledning kan gives, herunder muligheden for eventuel foster diagnostik, såfremt det ønskes. Vores DNA analyser gør det muligt at underbygge diagnosen ADOA ved fund af en mutation og især, når sygdomsbilledet er uklart, og man mistænker andre årsager til synsnervesygdom, kan dette bidrage til en afklaring.
Hvis miljøfaktorer påvises i samspil med en mutation, giver det mulighed for fremover at give en mere præcis prognose vedrørende udvikling af sygdommen hos den enkelte. Forebyggende individuel behandling kan sættes i gang, så man på lang sigt vil kunne mindske synstabet.
Hvorvidt årsagen til det forskellige udtryk i sygdomsfremtoningen skyldes genetiske faktorer eller, hvorvidt miljømæssige faktorer spiller ind, ved man endnu ikke. Vores studium vil bidrage til ny viden om dette, når sygdommens genetiske basis er bedre belyst.
På længere sigt vil kendskab til den genetiske baggrund for sygdommen bidrage til opklaring af de sygdomsfremmende mekanismer og herved lede forskningen hen imod udviklingen af nye behandlingsmetoder. Herunder genterapi samt eventuelt nye former for medicin.
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.