Grøn stær-patienter farer let vild i ’kopi-junglen’
Efter at øjendråberne Xalatan® mod grøn stær gik af patent i 2011, er fem kopiprodukter kommet på markedet. Flere studier har vist, at de tilgængelige kopiprodukter på mange måder er forskellige fra originalproduktet. Det gør det usikkert at navigere i ’kopi-junglen’ og svært at tro på, at
forskellene ikke smitter af på effekten.
Når et lægemiddel går af patent, står det andre producenter frit for at gå på markedet med kopiprodukter – såkaldte generika – til en billigere pris. Kopiprodukter skal leve op til de samme kvalitetskrav, men i langt de fleste tilfælde stiller Lægemiddelstyrelsen ikke krav til, at et kopipræparat skal testes i de samme effekt- og sikkerhedsstudier, som original-produktet har skullet for at blive godkendt til behandling. Vi har for nylig lavet et studie, der har undersøgt de kopiprodukter til øjendråberne Latanoprost (oprindeligt solgt under navnet Xalatan®), som findes på danske apoteker. Vores studie viser, at disse kopiprodukter langtfra altid er identiske med originalproduktet.
Kopiprodukter er kopier af godkendte lægemidler (originalprodukter) med samme aktive stof, koncentration og administrationsmåde. Kopiprodukter antages derfor at have den samme farmakologiske effekt og sikkerhedsprofil som det originalprodukt, de skal erstatte. Medicin beslægtet med prostaglandiner (en gruppe af hormonlignende stoffer, der er dannet ud fra fedtsyre og arachidonsyre) udgør 75 pct. af de recepter, der udskrives af danske læger til behandling af grøn stær. Heraf udgør de langt billigere kopiprodukter til lægemidlet Xalatan® (Latanoprost) 85 pct. af disse recepter.
Vi har undersøgt de forskellige Latanoprost-kopiprodukter ud fra otte sammenlignelige parametre, og set i forhold til originalproduktet fandt vi signifikante forskelle ved alle de
undersøgte kopiprodukter, for eksempel i pH-værdi, dråbestørrelse, viskositet (hvor tyktflydende øjendråberne er) og emballagens hårdhed. På apoteket får grøn stær-patienter automatisk udskrevet de billigste øjendråber, hvilket betyder, at de risikerer at få udleveret et ’anderledes’ produkt, hver gang de skal have nye øjendråber. Vores studie viser blandt andet, at der er forskel på, hvor mange kræfter det kræver at presse de forskellige kopi-øjendråber ud af emballagen. Da grøn stær-patienter ofte er ældre, lider mange af slidgigt, og de kan derfor have vanskeligt ved at administrere øjendråber i en emballage, som er hårdere – og dermed sværere – at presse en øjendråbe ud af.
Forvirrende forskelle
Xalatan® har, siden det kom i handlen, været det mest anvendte produkt til behandling af grøn stær. Siden det gik af patent i 2011, er flere Latanoprost-øjendråber blevet introduceret. Latanoprost-øjendråber indeholder det samme aktive stof (det stof, der har den virkende effekt) som Xalatan®. Ud fra dokumentation om kemisk- og farmaceutisk fremstilling, holdbarhed og renhed har Lægemiddelstyrelsen vurderet, at Latanoprost-øjendråber kan ordineres til grøn stær-patienter på lige fod med Xalatan®. Styrelsen har altså vurderet, at der opnås samme effekt hos patienter med grøn stær, hvad enten de får Xalatan® eller et Latanoprost-produkt. Det er derfor ofte tilfældet, at patienterne skifter mellem Xalatan® og de forskellige kopiprodukter uden at modtage særlige instrukser for det enkelte kopipræparat.
Når et originalprodukt skal godkendes til behandling af en sygdom eller symptomer, skal producenten kunne dokumentere, at det har den påståede virkning over for sygdommen eller symptomerne. Produktet skal i forsøg med mennesker leve op til de standarder for kvalitet, sikkerhed og effekt, som er fastsat og harmoniseret i EU. Kvalitet refererer til den kemiske og farmaceutiske kvalitet af det aktive stof og det færdige lægemiddel. Sikkerhed refererer til produktets bivirkningsprofil, mens effekt refererer til den ønskede kliniske virkning. I Danmark er det Lægemiddelstyrelsen, der afgør, om et lægemiddel lever op til de fastsatte krav om kvalitet, effekt og sikkerhed.
Kopiprodukter skal ikke igennem de samme godkendelsesprocedurer, da kvaliteten, effekten og sikkerheden allerede er dokumenteret og godkendt for originalproduktet. Og producenten af et kopiprodukt kan således henvise til disse studier. Kopiprodukter skal i stedet afprøves i mindre studier, der skal dokumentere, om de er bioækvivalente med originalproduktet. At kopiprodukter er bioækvivalente, vil sige, at de har samme aktive stof i samme lægemiddelform og styrke som originalproduktet. Kopiprodukter kan godkendes som erstatning for et originalt produkt, hvis optagelsen af det – hvad angår mængde og hastighed – med 90 pct. sandsynlighed ligger mellem 80 og 125 pct. i forhold til originalproduktet.

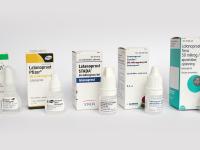
Myndighederne stiller ikke krav til, at produkternes emballage har en bestemt form og farve eller er fremstillet af bestemte materialer. Ud over den uhensigtsmæssige konsekvens af, at der skal forskellig styrke til at presse dråberne ud af emballagerne, mener vi, at det kan være meget forvirrende for en ældre patient at skifte produkt hele tiden. Den ene måned er emballagen måske blå, og flasken cylinderformet, mens den måneden efter er grøn og har en anden form.
Myndighederne stiller ikke krav til, at produkternes emballage har en bestemt form og farve eller er fremstillet af bestemte materialer.
Vores studie har ikke undersøgt koncentrationen af det aktive stof, når det kommer ud af emballagen, men vi håber, at vi i fremtiden – i samarbejde med nogle af vores kemikere – kan få denne viden. Aktuelt stilles der kun krav til koncentrationen af det aktive stof i det produkt, der fyldes på dråbeflaskerne, men ingen krav til koncentrationen i dråberne, når de kommer ud, da det antages at være den samme. Vores frygt er, at der vil være stor forskel. For det vil i så fald kunne influere på produkternes kvalitet og deres evne til at holde grøn stær i ave.
Mange usikre faktorer
Et patent løber i op til 20 år. Hvad angår lægemidler, kan et patent i nogle tilfælde forlænges. Et patent kan siges at være en virksomheds kontrakt med samfundet: Virksomheden offentliggør information om den nye opfindelse mod at få et tidsbegrænset monopol. Proceduren for udviklingen af nye lægemidler er typisk, at lægemiddelvirksomheden først finder frem til det aktive stof, som skal have den virkende effekt i lægemidlet, hvorefter det efterfølgende arbejde består i at arbejde med for eksempel fremstilling og dosering. Derfor er det ikke ualmindeligt, at virksomheden først tager patent på det aktive stof for så noget tid senere at få patent på den del af lægemiddeludviklingen, der knytter sig til for eksempel fremstillingen af lægemidlet eller et særligt doseringsregime. Da det primære og de sekundære patenter opnås med tidsforskydning, udløber de også med tidsforskydning. Så snart patentet på det aktive stof udløber, har konkurrerende virksomheder som udgangspunkt ret til at påbegynde salg af kopiprodukter.
Vores studie har vist, at de opløsningsmidler, som de eksisterende kopiprodukter indeholder, ikke er ens fra produkt til produkt. De har blandt andet en forskellig pH-værdi, hvilket kan have indflydelse på, hvor effektivt det aktive stof i lægemidlet er. Vi har vist, at viskositeten i de forskellige Latanoprost-kopiprodukter ikke er ens. Og endeligt har vi dokumenteret, at dråbestørrelserne og den totale mængde af medicin i de forskellige kopiprodukter er forskellig.
Om end vi har vist tydelige forskelle på de eksisterende Latanoprost-kopiprodukter, kan vi ikke sige, om de forskelle, vi har målt, har konsekvenser for, hvor godt de virker, og hvor sikre de er for patienterne at bruge. Vi kan dog konstatere, at ’kopi-junglen’ er svær for patienterne at navigere i. Det er derfor meget forståeligt, hvis de bliver kede af det og frustrerede over, at det ikke er nemt at finde hoved og hale i kopiprodukter. Selv om vi ikke ved, om forskellene er kvalitetsforringende, er det umiddelbart svært at tro, at de dokumenterede forskelle ikke på den ene eller den anden måde smitter af på effekten.
Når det er sagt, kan vi ikke afvise, at nogle af de nye kopiprodukter – måske grundet deres reducerede surhedsgrad – har bedre effekt og færre bivirkninger end Xalatan®. Aktuelt er vi ved at sætte et nyt studie op, der skal undersøge effekten af kopiprodukter på nogle af cellerne på øjets overflade.
Overordnet er det vigtigt at fastslå, at formålet med denne artikel ikke er at dømme kopiprodukter ude. Der er rigtig meget positivt at sige om kopiprodukter. De bryder originalprodukters monopol og skaber konkurrence på markedet, da kopiprodukter er billigere end originalproduktet. Med denne artikel vil vi dog opfordre til, at kravene til introduktionen af nye kopiprodukter ses efter i sømmene. De billigere alternativer skal have samme påviste effekt og bivirkningsprofil som originalproduktet, så de lever op til de strenge krav, myndighederne stiller til introduktion af nye lægemidler.
Læs mere: Acta Ophthalmol (juni 2017) Kolko M og Jensen PK: The physical properties of generic latanoprost ophthalmic solutions are not identical (side 370-373).
Hvert år bruger 1/2 million danskere vores viden om synet. Vi er glade for at tilbyde forskningsbaseret viden om synet til dig - helt gratis. Det vil vi gerne blive ved med. Derfor har vi brug for din hjælp. Gør ligesom tusindvis af andre.







